4.2 Estructura y función de la cadena respiratoria
La cadena respiratoria se abastece de poder
reductor
Las células eucariotas y procariotas obtienen
energía, principalmente bajo forma de ATP, a partir del poder reductor (o H2)
presente en las moléculas de glúcidos, lípidos y aminoácidos, entre otras. El
aceptor final de los H2 es el O2, se trata de un ejemplo de célula aerobia. Sin
embargo, hay otros tipos de células en que los aceptores finales de H2 son
moléculas diferentes del O2, esas células son anaerobias y fermentativas. Ahora
vamos a centrar el estudio en células aerobias.
• Los azúcares, ácidos grasos y aminoácidos
cuando son oxidados (degradados) proveen de poder reductor, de manera más o
menos directa, a la cadena respiratoria (Figura 1). Así, se reducen cofactores
como el NAD y el FAD dando inicio a la transferencia del poder reductor (H2) hasta
el aceptor final, que en los organismos aerobios es el O2 (Figura 1).
• La variación de energía de los electrones
desde los precursores reducidos (aminoácidos, glúcidos y ácidos grasos) hasta
el agua, es un proceso exergónico, que impulsa la reacción endergónica de
síntesis de ATP a partir del ADP y P.
La cadena respiratoria en las células
eucariotas ocurre en mitocondrias
• La mitocondria en un organelo presente en las
células de vegetales, animales y hongos, es decir en todas las eucariotas. Su número
por célula es variable, y está limitada por dos membranas, una externa y otra
interna. Estas membranas delimitan dos espacios: la cámara externa o espacio intermembranal
y la matriz.
• En la membrana interna se localiza la cadena
respiratoria, que consta de una serie de transportadores de electrones como el
NAD, CoQ, citocromos y diversas enzimas. En las bacterias la cadena
respiratoria está asociada a la membrana celular.
• La cadena respiratoria siempre está asociada
a una membrana, porque para su funcionamiento es necesario un ordenamiento
espacial bien definido de los transportadores y proteínas que la integran, como
se verá más adelante.
Los transportadores de cadena respiratoria
tienen diferente afinidad por los electrones
A través de la cadena respiratoria se dan
reacciones de óxido reducción que se suceden desde el NAD y el FAD hasta el
oxígeno (Fig. 5). Los electrones pueden ser captados o cedidos de diferentes
formas:
a. un electrón individualmente,
b. un electrón unido a un protón; como un átomo
de H,
c. dos electrones unidos a dos protones; como
dos átomos de H.
En la figura 5 se representan los
transportadores de la cadena respiratoria ordenados según su potencial redox.
La dirección del flujo de e-, indicada con una flecha, es desde los
transportadores con menor afinidad por los e- (potencial redox más
electronegativo) a los de mayor afinidad (potencial redox más electropositivo).
La cadena respiratoria está integrada por
trasportadores y proteínas que forman
los “complejos”
Una forma de analizar el funcionamiento de la
cadena respiratoria es a través de los complejos que forman los transportadores
y las enzimas.
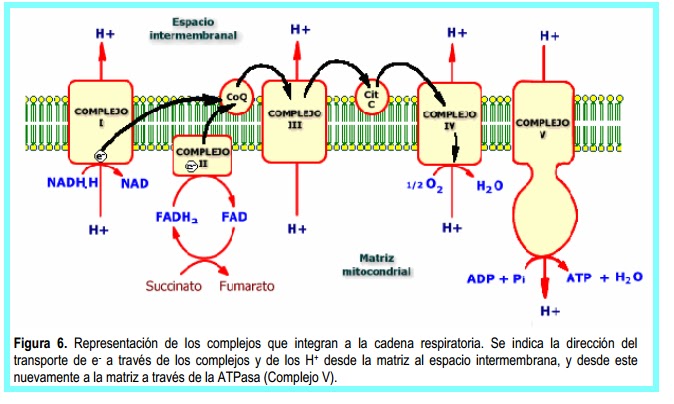
• El Complejo I (NADH - ubiquinona reductasa)
es por donde ingresan la mayoría de los electrones
a la cadena. Los electrones son
transferidos desde el NADH.H a la CoQ (Fig. 6), a través del FMN (flavín
mononucleótido) que es parte del Complejo I. El esquema resume el proceso.
El Complejo II (succinato deshidrogenasa) es el
otro punto de entrada de electrones a la cadena (Fig. 6), y en su transferencia
entre el FAD y la CoQ no libera energía suficiente para bombear protones. Por
esto se genera un ATP menos cuando la cadena comienza por el FAD respecto a cuando
comienza por el NAD.
• El Complejo III (CoQ - citocromo c reductasa)
recibe electrones de los Complejos I y II (Fig. 5 y 6). A partir de este paso
se transportan electrones, y quedan libre los H+. El Complejo III involucra a
los citocromos y la energía aportada por este Complejo para el bombeo de
protones es suficiente para formar ATP (Fig. 7).
El Complejo IV (citocromo oxidasa) cataliza la
formación de H2O a partir de los 2 e-, ½ O y 2H+.
Este complejo contribuye con la generación de
un gradiente de protones suficiente para generar un ATP. Observar que el
oxígeno se reduce a agua, mientras la energía liberada por los electrones
permite la fosforilación del ADP a ATP: el proceso se denomina fosforilación oxidativa.
• El Complejo V, también anclado en la membrana
mitocondrial interna, es la ATPasa o ATPsintasa (Fig. 6). Este complejo está
formado por los componentes Fo y F1:
a. Fo
corresponde al canal protónico (Fig. 7). En presencia de oligomicina, un
antibiótico que se une a este canal, no ocurre el pasaje de H+, y por lo tanto
se inhibe la síntesis de ATP.
b. F1 contiene las unidades catalíticas de la
ATPasa, que permite sintetizar el ATP a partir del ADP y P (Fig. 6 y 7).
La teoría quimiosmótica explica cómo el
gradiente protónico generado por la cadena respiratoria permite la síntesis de
ATP
La energía liberada por los electrones en la
cadena respiratoria, es usada para el bombeo de protones desde la matriz
mitocondrial hacia el espacio intermembranal (figuras 4 y 8). Este bombeo
produce un gradiente de protones, y como consecuencia una desigualdad de cargas
y de pH a ambos lados de la membrana interna.
• Como consecuencia del bombeo de H+, el pH de
la matriz se vuelve alcalino respecto al del espacio intermembranal y se genera
un gradiente químico y eléctrico. La fuerza protón motriz, consecuencia del
gradiente, hace posible que los protones vuelvan a la matriz, de manera
que el pH tiende a igualarse a ambos
lados de la membrana.
• A medida que los H+ fluyen pasivamente de
nuevo hacia la matriz a través del canal Fo, el complejo enzimático ATP sintasa
utiliza la fuerza protón motriz para generar el enlace fosfoahidro entre el ADP
y el P, y producir ATP.
• La membrana interna es impermeable a los
iones, incluyendo a los H+, que sólo pueden atravesarla mediante
transportadores y por canales Fo - F1 (ATP sintasa).
Referencias:








:0
ResponderEliminar